Les différents types de prélèvements
Trois types de prélèvements peuvent être réalisés dans un contexte de diagnostic :
Le plus souvent, un prélèvement sanguin
Plus rarement, une biopsie cutanée
Exceptionnellement une pièce anatomique,
Le prélèvement sanguin a pour objectif d’obtenir de l’ADN (isolé à partir du noyau des cellules sanguines) pour faire une recherche de mutation.
La biopsie cutanée est mise en culture pour obtenir des fibroblastes, cellules qui synthétisent les différentes protéines de la matrice extracellulaire.
A partir de la culture de fibroblastes, différentes études pourront être entreprises :
Le 3ème prélèvement est la pièce anatomique, prélevée au cours d’une intervention chirurgicale. Le plus souvent il s’agit d’un fragment d’aorte récupéré lors d’une intervention de remplacement de l’aorte ascendante. Ce fragment est utilisable pour différents traitements et types d’examens :
• un examen histologique de routine pour évaluer la qualité de l’aorte (étude au microscope après coupe et coloration).
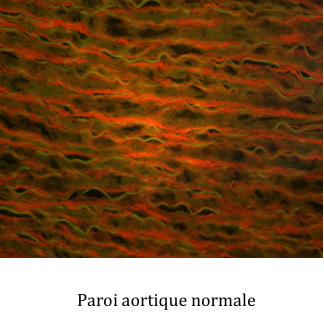
• congélation immédiate et étude ultérieure de structures et de composants particuliers du tissu;
• traitement immédiat pour mise en culture des cellules musculaires lisses de la paroi de l’aorte. Ces cellules assurent la synthèse des composants de la matrice extracellulaire.
Ces deux dernières techniques sont surtout utilisées en recherche.
Contexte réglementaire
Parmi tous ces examens, certains sont utilisés pour le diagnostic, d’autres uniquement dans le cadre d’activités de recherche. Les prélèvements pour réaliser ces examens sont soumis à des réglementations différentes.
Analyse d’ADN
Quel que soit le type de prélèvement, s’il a pour objectif une analyse d’ ADN, il ne pourra être prescrit qu’au cours d’une consultation par un médecin généticien ou par un médecin d’une autre spécialité mais appartenant à une consultation multidisciplinaire déclarée auprès des autorités sanitaires régionales et nationales. Le médecin devra informer son patient du type de prélèvement, du ou des examens qui seront réalisés et dans quel but. Une fois cette information donnée, un formulaire de consentement doit être signé et fourni au laboratoire avec le prélèvement. Le patient conservera une copie de ce formulaire de consentement. Dans quelques cas, le médecin pourra être amené à proposer un formulaire d’un autre type appelé formulaire de non opposition. Ce type de formulaire permet de recueillir le consentement pour la réalisation d’examens divers qui pourraient éventuellement être réalisés, mais dont la nature précise n’est pas déterminée au moment où le prélèvement est réalisé. En pratique, ce type de consentement “ a priori ” est utilisé pour des pièces anatomiques voire des biopsies.
Recherche
Pour les prélèvements réalisés dans le contexte d’un protocole de recherche, les formalités sont comparables : information du patient par l’un des médecins participant au protocole de recherche, signature d’un consentement.
Rendu des résultats
Le résultat d’un examen à visée diagnostique sera rendu, par le laboratoire de biologie moléculaire qui l’a réalisé, uniquement au médecin prescripteur. C’est le médecin prescripteur qui est chargé de le rendre au patient au cours d’une nouvelle consultation.
S’il s’agit d’un prélèvement utilisé pour la recherche, il n’y aura pas de résultats personnel à rendre le plus souvent, mais les personnes qui participent à des recherches sont tenues au courant des résultats acquis.
Transfert des prélèvements au laboratoire exécutant
Le délai maximal de transmission du prélèvement au laboratoire dépend du type d’examen qui sera réalisé.
En pratique courante, c’est l’analyse de l’ADN qui est la plus fréquente : le prélèvement sanguin devra être transmis dans les 24 à 48 heures suivant la prise de sang. Le transport sera réalisé à température ambiante, par transporteur soit interne (navette entre hôpitaux publiques d’une même ville) soit externe (services postaux, transporteurs privés…).
Pour les autres prélèvements, ceux-ci devront généralement parvenir dans les plus brefs délais dans le service qui va les étudier. Parfois le traitement de l’échantillon commence au moment de son prélèvement.
Prise en charge des examens réalisés à des fins diagnostiques
La nomenclature des actes de génétique moléculaire n’est précise que pour un nombre limité de maladies héréditaires. Pour toutes les autres maladies, il existe un tarif forfaitaire de base codifié à B 500 (soit 500 x 0,27 euros = 135 euros). Les actes sont totalement remboursés et donc sont accessibles à tous les assurés. Par contre, ce tarif forfaitaire est très en-dessous du coût réel d’une étude moléculaire lorsqu’il faut explorer de très grands gènes (comme le gène FBN1 impliqué dans le syndrome de Marfan) et/ou plusieurs gènes. De ce fait, les laboratoires référents reçoivent des crédits ministériels spécifiques ( crédits D.H.O.S. pour Direction de l’Hospitalisation et de l’Organisation des Soins) permettant de couvrir la différence de coût.
Quel type de laboratoire réalise les études de génétique moléculaire?
L’étude de gènes dans un contexte de diagnostic est réservée à des laboratoires et des biologistes qui sont agréés par les autorités sanitaires. L’objectif de cet agrément est d’encadrer ces activités nouvelles et coûteuses, de s’assurer de la compétence des biologistes réalisant les actes et, par la visite du laboratoire, s’assurer que les conditions réglementaires (locaux, matériel, personnel, procédures de qualité…) sont remplies et donc garantissent la qualité des examens réalisés.
Une fois l’agrément obtenu, il couvre l’étude de tous les gènes. La majorité des centres et biologistes agréés sont publiques, hospitaliers. En pratique, la plupart des laboratoires n’analysent qu’un nombre limité de gènes. Le choix des gènes étudiés est le reflet de plusieurs éléments :
– le rapport coût / bénéfice pour la prise en charge du malade,
– les compétences propres développées par les biologistes dans un groupe de pathologies,
– les besoins locaux ou régionaux.
Etapes du diagnostic par génétique moléculaire
L’étude d’un prélèvement comprend plusieurs étapes. Il faut d’abord extraire l’ADN des globules blancs, puis vérifier sa qualité et la quantité obtenue.
A l’issue de cette première étape, si des conditions de qualité et de quantité ne sont pas remplies, un nouveau prélèvement est demandé.
Une fois l’ADN obtenu, les 65 exons (c’est-à-dire les régions de l’ADN contenant l’information nécessaire à la production de la protéine fibrilline-1) du gène FBN1 sont analysés, base à base à la recherche d’une mutation. Cette recherche est techniquement longue, comportant un certain taux d’échec et encore relativement peu automatisée. Elle nécessite donc un temps important de technicien pour étudier chaque prélèvement. Une fois une altération trouvée, le biologiste intervient. Son rôle est d’évaluer s’il s’agit bien de la mutation responsable de la maladie ou bien d’une variation sans grande conséquence sur la fonction du gène ou de la protéine.
Mutations non-sens / mutations faux-sens / polymorphismes
De façon schématique, on observe deux grands types d’altération selon leur effet sur la production de la protéine :
– soit on observe une mutation non-sens (ou mutation codon Stop prématuré) conduisant à l’apparition anormalement précoce d’un signal de fin de synthèse de la nouvelle protéine synthétisée. Cette situation est la plus simple car la conséquence de la mutation est claire : elle ne nécessite pas d’examen supplémentaire puisque l’altération est par son essence même une mutation pathogène (responsable d’une pathologie).
– soit on observe une variation faux-sens conduisant au remplacement d’un seul acide aminé par un autre acide aminé (les protéines sont constituées de briques élémentaires appelées acides aminés) dans la protéine. Alors les conséquences de cette modifications ne sont pas aussi claires. Il va falloir alors trancher entre une mutation pathogène responsable de la maladie ou une simple variation sans effet pathologique (polymorphisme).
Pour conclure dans un sens ou dans l’autre, il faudra accumuler les arguments supplémentaires :
Mutation sporadique
L’une des informations les plus sures que puisse apporter la génétique moléculaire dans le syndrome de Marfan est le caractère « sporadique » de la mutation. On parle de mutation sporadique si les parents biologiques du patient ne portent pas cette mutation ; alors une nouvelle mutation (néo-mutation) est apparue dans un des gamètes (spermatozoïde ou ovocyte) dont le patient est issu, ou très tôt au cours du développement embryonnaire.
Ce type d’évènement est fréquent dans le gène FBN1. il permet de comprendre pourquoi plus de 25 % des malades n’ont aucun apparenté malade. Pour les parents d’un enfant atteint d’une forme sporadique de syndrome de Marfan le risque d’avoir un deuxième enfant atteint de ce syndrome est quasi-nul.
Quel est l’intérêt de rechercher une mutation?
Il est important de re-souligner que le diagnostic de Marfan reste essentiellement une démarche clinique. Par ailleurs, une fois le diagnostic posé chez un sujet, la caractérisation de la mutation n’a pas d’intérêt pour la prise en charge, le suivi et ne fournit aucun élément prédictif quant à l’évolution et la gravité de la maladie.
Par contre, la recherche d’une mutation aura toute son importance dans ces cas : – Pour un premier diagnostic de syndrome de Marfan dans une famille : lorsque le diagnostic clinique reste incertain après un examen multidisciplinaire, la mise en évidence d’une mutation permettra d’affirmer le diagnostic. Mais attention : même si aucune mutation n’est retrouvée, le diagnostic de “ Marfan ” ne pourra être éliminé. En effet toute technologie à ses limites et peut apporter des résultats faussement négatifs. .
– Pour le diagnostic chez des apparentés d’un sujet chez lequel le diagnostic clinique a été établi. La mutation sert alors de marqueur de la maladie, particulièrement utile pour confirmer ou infirmer le diagnostic chez des sujets ayant peu ou pas de symptômes (notamment les enfants puisque la maladie peut n’apparaître qu’au cours de l’adolescence).
– dans le cadre de l’assistance médicale à la procréation, la mise en évidence de la mutation est un préalable technique indispensable (Voire paragraphe DPN – DPI)
Il ressort donc que, en pratique, la recherche de mutation sera réalisée dans des circonstances variables et sera toujours précédée d’un dialogue entre clinicien et biologiste pour en évaluer l’intérêt diagnostique.
Et il faudra combien de temps pour avoir le résultat?
Il n’y a pas de réponse simple à cette question. La plage de temps est variable allant de 15 jours à plusieurs années avec des “ moyennes cibles ” de 12 mois pour une première recherche de mutation dans une famille et de 2 mois pour une recherche de mutation déjà connue chez un sujet apparenté.
Comment expliquer une telle variation ? En prenant en compte les éléments suivants : le temps minimal nécessaire pour réaliser les différentes étapes actuelles du diagnostic génétique exposées plus haut, le nombre de techniciens réalisant ces étapes, le nombre de biologistes analysant les résultats, le nombre de secrétaires gérant le travail et rédigeant les compte-rendus, le nombre de demandes reçues par un laboratoire.
Pour un diagnostic en urgence réalisé par un technicien et analysé par un biologiste, il faut environ 15 jours lorsque la mutation familiale est connue. Ceci représente une situation idéale qui en pratique ne sera mise en oeuvre que lorsqu’un diagnostic devra être réalisé en extrême urgence (cas très rare dans des circonstances particulières dont le diagnostic prénatal).
En pratique courante, les demandes reçues par les laboratoires sont supérieures voire largement supérieures aux capacités de réponse des laboratoires. Les biologistes gèrent donc en permanence un équilibre fragile pour répondre aux demandes avec les moyens dont ils disposent. Des évolutions techniques ont déjà permis d’améliorer le diagnostic moléculaire tant du Marfan que de toutes les autres maladies héréditaires puisqu’il y a 15 ans, le laboratoire d’Ambroise Paré avait étudié en une année tout le gène FBN1 chez 15 sujets (utilisation de techniques manuelles par un technicien) alors qu’en 2011, 5 techniciens ont étudié tout le gène FBN1 chez 235 sujets, tout le gène TGFBR2 chez 185 sujets et ont réalisé la recherche d’une mutation connue chez plus de 350 apparentés. A cela il faut ajouter l’étude d’environ une dizaine d’autres gènes dans des formes particulières de maladies apparentées (voir chapitre syndromes apparentés).
Seule l’évolution des techniques et leur automatisation permettront d’augmenter encore le nombre de sujets analysés par an et de diminuer de façon encore plus marquante le délai de rendu des résultats.
